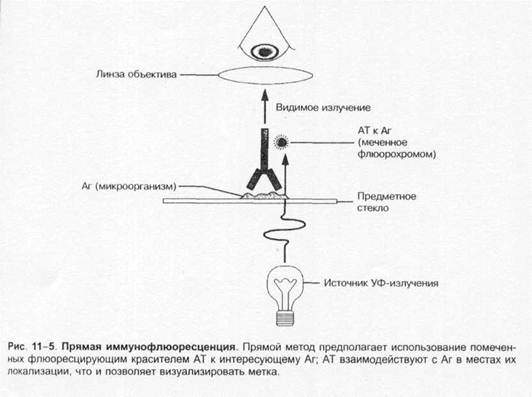
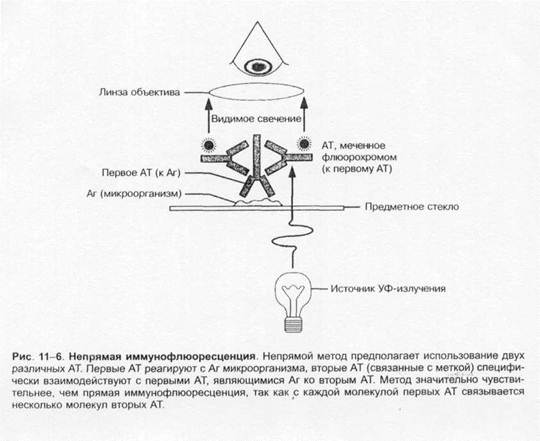
Окрашенные препараты
![]() Для приготовления окрашенных препаратов из исследуемого объекта готовят мазки и фиксируют их.
Для приготовления окрашенных препаратов из исследуемого объекта готовят мазки и фиксируют их.
Отбор материала.
Тампоны, содержащие микроорганизмы, прокатывают по предметному стеклу (рис. 1-8,
А); с их помощью также готовят мазки из непрозрачных жидкостей, например взвеси испражнений (рис. 1-8,
Б). Мазки из материалов со слизистой или грубой консистенцией готовят растиранием их между двумя предметными стёклами (рис. 1-9).
Прозрачные жидкости (например, мочу или СМЖ) можно нанести в виде капли на предметное стекло (рис. 1-10, А),
при этом границы капли желательно обвести маркёром. Лучшие результаты даёт предварительное центрифугирование; затем осадок наносят на стекло; если он густой, его можно распределить с помощью стеклянной палочки (рис. 1-10, Б).
Фиксация.
В практической бактериологии наиболее распространена термическая фиксация
(над пламенем горелки) — метод грубый, но сохраняющий морфологию и отношение к красителям у бактерий. Для более детального изучения структуры клеток применяют фиксирующие растворы,
предотвращающие ферментативный аутолиз бактерий и стабилизирующие макромолекулы путём химического их сшивания. Для светооптической микроскопии используют формалин, спирты, глутаральдегид, жидкость Карнуа, ацетон, пары осмиевой кислоты и др. Мазки фиксируют, помещая их в раствор фиксатора или нанося фиксаж на мазок. Для электронной микроскопии применяют глутаральдегид и тетраоксид осмия.
Окрашивание.
Стандартные красители, используемые для окраски бактерий, — карболовый фуксин Циля, фуксин Пфайф-фера и метиленовый синий по Лёффлеру. Для получения более информативных результатов в светооптической микроскопии используют специальные и дифференцирующие методы окраски.
|
|
|
|
Специальные методы окраски бактерий.
Наибольшее распространение нашли методы Грама и Циля-Нильсена (рис. 1-11).
Дифференцирующие методы
обычно применяют для окрашивания различных морфологических структур.
Капсулы. Для окраски капсул бактерий применяют методы Хисса, Лейфсона и Антони; последний метод наиболее прост и включает окраску кристаллическим фиолетовым с последующей обработкой 20% водным раствором CuSO4.
Жгутики. Для окраски жгутиков предложены методы Лёффлера, Бейли, Грея и др. Для этих методов характерны первоначальное протравливание препарата [обычно растворами таннина, KAl(SO4)2, HgCl2] и последующая окраска (чаще карболовый фуксин Циля).
Споры. Окраску спор бактерий проводят после предварительной обработки их стенок. Наиболее прост метод Пешкова, включающий кипячение мазка с синькой Лёффлера на предметном стекле с последующей докраской нейтральным красным. Споры окрашиваются в синий цвет, вегетативные клетки — в розовый.
Проведение ПЦР в разных объемах смеси в пробирках
Перед проведением реакции в микроплашках ПЦР провели в пробирках Eppendorf с общим объемом смеси 5, 4, 3, 2 и 1 мкл (исходная концентрация ДНК – 7 нг) в среде масла. Подобная модель миниатюризации реакции может дать ответ на вопрос в каком минимальном объеме возможно прохождение амплификации и насколько эффективно. Данные о приросте сиг ...
История развития анатомии (научная анатомия – после
XVI века).
Анатомия – наука о происхождении и развитии, формах и строении человеческого организма. Слово «анатомия» происходит от греческого «анатемно» - рассекать, расчленять.
Это название определяется тем обстоятельством, что первоначальным и основным методом, с помощью которого анатомия добывала фактический материал, относящийся к внутреннему ...
Показатели минерального обмена в плазме крови
Клиническое значение
Кальций Пониженное содержание кальция наблюдается при гипопаратиреозе, нарушении всасывания кальция, недостатке витамина D, при рахите, почечной недостаточности.
Повышенное содержание кальция отмечено при гиперпаратиреозе, гипертиреозе, злокачественных опухолях с метастазами в кости, при гипервитаминозе D. Опасным ...