Изоэлектрическое фокусирование и изотахофорез
Фокусирующий ионный обмен. Этот метод часто наз. электрофоретич. фокусировкой или просто электрофокусированием, связан с наложением градиента концентрации или рН р-ра параллельно электрич. полю. Благодаря этому разделяемые ионы могут изменять величину и знак заряда по мере перемещения в поле градиента. При этом в фиксир. точках системы каждый компонент переходит в изоэлектрич. состояние, в к-ром ср. заряд частиц данного компонента равен нулю. Упомянутые точки являются местом концентрирования (фокусирования) отдельных компонентов смеси (рис.5). Положение зон фокусирования определяется градиентом концентрации комплексообразующего реагента или рН р-ра и константами устойчивости комплексных ионов разделяемых элементов. При разделении смеси белков или др. амфотерных соед. положение зон определяется значениями их изоэлектрич. точек.
Для создания градиента рН электродные камеры заполняются буферными р-рами с разными значениями рН. Напр., для разделения редкоземельных элементов цериевой группы в 0,001 М р-ре этилендиаминтетрауксусной к-ты рН должен изменяться по длине колонки от 1,7 у анода до 2,4 у катода.
В сер.60-х гг.20 в. было предложено создавать градиент рН с помощью амфолитов - смесей алифатич. полиаминокислот. Под влиянием электрич. поля амфолиты распределяются в соответствии со своими изоэлекгрич. точками и тем самым образуют градиент рН. Применение амфолитов позволяет добиться весьма высокой разрешающей способности метода: в нек-рых случаях удается разделить белки, изоэлектрич. точки к-рых различаются на 0,02 единицы рН.
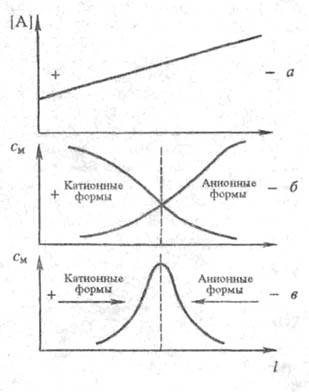
Схема, поясняющая метод электрофокусирования: а - образование градиента концентрации лиганда [А] ; б - распределение ионных форм мигранта; в - концентрирование лиганда в узкой зоне; см - концентрация мигранта.
Описанный метод, являясь самостоятельным, в то же время представляет собой вариант зонного электрофореза. Во всех модификациях последнего идентификацию и количеств. определение в-в в зонах можно проводить как непосредственно на носителе, так и после элюирования. В обоих случаях используют методы радиоактивных индикаторов, фотометрию в прямом и отраженном свете, люминесцентный анализ.
Фронтальные методы основаны на измерении скорости перемещения границы раздела р-ров с разной плотностью. Классич. вариант метода был разработан в 1930 и с тех пор применяется для определения подвижности и разделения высокомол. в-в, в частности белков. В простейшей модификации метода в U-образную трубку помещают р-р белков, а над ним буферный электролит, в к-рый погружены электроды. При наложении электрич. поля индивидуальные белки перемещаются с разл. скоростями, образуя серию границ. Их положение регистрируют оптич. методами по изменению коэф. преломления.
Изотахофорез. Осн. частью прибора служит капиллярная трубка с анодным и катодным резервуарами на концах. При анализе анионов анодное отделение и капилляр заполняют т. наз. лидирующим электролитом, содержащим анион с высокой подвижностью. Ср. скорость миграции анионов в этом электролите должна быть выше подвижности любого аниона в исследуемой смеси. Катодное отделение заполняют т. наз. замыкающим электролитом, анион к-рого имеет подвижность меньшую, чем подвижность любого др. аниона в смеси. Анализируемый образец, в к-ром нужно определить содержание анионов, вносят между предшествующим и замыкающим электролитами. После подачи напряжения (5-10 кВ) при силе тока до 100 мкА по мере движения анионов к катоду постепенно образуются зоны индивидуальных анионов определенной длины, разделенные четкими границами, ширина к-рых составляет 0,2-0,3 мм при диаметре капилляра 0,1 мм. После этого все зоны будут перемещаться с одинаковой скоростью (отсюда назв. метода). Соотношение концентраций анионов в двух соседних зонах с1 и с2 в установившемся режиме будет определяться выражением Кольрауша:
с1/с2 = n1/n2, (4)
где n1и n2 - числа переноса.
При анализе катионов лидирующий электролит должен содержать катионы с высокой подвижностью, замыкающий - с миним. для данной системы скоростью миграции.
Кол-во в-ва в зоне Q и ее длина l в капилляре постоянного сечения S связаны простым соотношением:
Q = ClS, (5)
где С - коэф. пропорциональности.
В установившеся режиме градиент потенциала при переходе от лидирующего к замыкающему электролитам скачкообразно возрастает в соответствии с подвижностью ионов, составляющих данную зону. Это приводит к температурным скачкам между зонами, регистрируя к-рые с помощью термопары можно определить расстояние между зонами и по выражению (5) найти кол-во в-ва в зоне.
Наличие собственной программы развития системы и
способность к активному оперированию информацией
Всем живым системам любого уровня сложности, как организменным„ так и надорганизменным, совершенно независимо от их функционально-структурных особенностей, элементарной основы и всех других качеств, свойственно наличие определенной собственной программы развития, реализация которой обеспечивает сохранение системы в меняющихся условиях в ...
Доказательство роли ДНК в наследственности
1) Трансформация бактерий. (В 1928 г впервые получили доказательство возможности передачи наследственных задатков от одной бактерии к другой. Вводили мышам вирулентный капсульный и авирулентный бескапсульный штаммы пневмококков. При введении вирулентного штамма мыши заболели пневмонией и погибли. При введении авирулентного штамма – живы ...
Экологические проблемы современности.
Человечество слишком медленно подходит к пониманию масштабов опасности, которую создает легкомысленное отношение к окружающей среде. Между тем решение (если оно еще возможно) таких грозных глобальных проблем, как экологические, требует неотложных энергичных совместных усилий международных организаций, государств, регионов, общественност ...
