Каталитические системы дыханияСтраница 1
Окисление дыхательных субстратов в ходе дыхания осуществляется с участием ферментов. Ферменты как белковые катализаторы, помимо свойств, присущих неорганическим катализаторам, обладают рядом особенностей: высокой активностью, высокой специфичностью по отношению к субстратам и высокой лабильностью. Их пространственная организации зависящая от нее активность изменяются под действием внешних и внутренних факторов. Эти свойства обеспечивают возможность тонкой регуляции обмена веществ на уровне ферментов.
Типы окислительно-восстановительных реакций.
Существуют четыре способа окисления, и все они связаны с отнятием электронов:
1) непосредственная отдача электронов, например:
![]()
2) Отнятие водорода:
![]()
3) присоединение кислорода:
![]()
4) образование промежуточного гидратированного соединения с последующим отнятием двух электронов и протонов:
![]()
Оксидоредуктазы.
Поскольку окисление одного вещества (донора электронов и протонов) сопряжено с восстановлением другого соединения (их акцептора), ферменты, катализирующие эти реакции, называют оксидоредуктазами. Все они относятся к I классу ферментов:
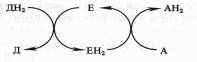
Донор (Д) отдает электроны и протоны, акцептор (А) принимает их, а энзим (Е) осуществляет реакцию переноса. Существуют три группы оксидоредуктаз:
а) анаэробные дегидрогеназы передают электроны различным промежуточным акцепторам, но не кислороду;
б) аэробные дегидрогеназы передают электроны различным акцепторам, в том числе кислороду;
в) оксидазы способны передавать электроны только кислороду.
Анаэробные дегидрогеназы.
Это двухкомпонентные ферменты, коферментом которых может быть НАД+ (никотинамидадениндинуклеотид):
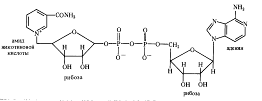
При окислении субстрата НАД+ превращается в восстановленную форму НАДH, а второй протон субстрата диссоциирует в среду (НАДH+ Н+). К анаэробным НАД-зависимым дегидрогеназам относятся такие ферменты, как алкогольдегидрогеназа, лактатдегидрогеназа, малатдегидрогеназа и др. Коферментом анаэробных дегидрогеназ может быть также НАДФ+ (никотинамидадениндинуклеотидфосфат), содержащий на одну фосфатную группировку больше, чем НАД + . НАДФ- зависимыми дегидрогеназами являются изоцитратдегидрогеназа, глюкозо-6-фосфатдегидрогеназа, 6-фосфоглюконатдегидрогеназа и др.
Субстратная специфичность фермента зависит от его белковой части. Многие НАД- и НАДФ-зависимые дегидрогеназы нуждаются в присутствии ионов двухвалентных металлов. Например, алкогольдегидрогеназа содержит ионы цинка.
Окисленные и восстановленные формы коферментов анаэробных дегидрогеназ могут взаимопревращаться в реакции, катализируемой ферментом НАД(Ф)-трансгидрогеназой:
НАДФH + НАД+ = НАДФ+ + НАДH
Анаэробные дегидрогеназы передают водород, т. е. электроны и протоны, различным промежуточным переносчикам и аэробным дегидрогеназам.
Аэробные дегидрогеназы.
Это также двухкомнонентные ферменты, получившие название флавиновых (флавопротеины).
Помимо белков, в их состав входит прочно связанная с ними простетическая группа — рибофлавин (витамин В2).
Различают два кофермента этой группы: флавинмононуклеотид (ФМН), или желтый дыхательный фермент Варбурга, и флавинадениндинуклеотид (ФАД).
ФМН (рибофлавин-5-фосфат) содержит гетероциклическое азотистое основание — диметилизоаллоксазин, спирт рибит (производное рибозы) и фосфат:
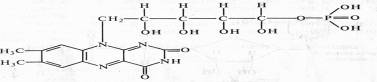
В ФАД кроме ФМН имеется еще один нуклеотид — аденозинмонофосфата:
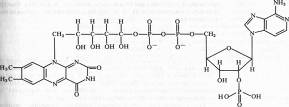
Активной группой в реакции присоединения и отдачи электронов и протонов в ФМН и ФАД служит изоаллоксазин. Взаимодействие с восстановленным переносчиком, например НАДH, происходит следующим образом:
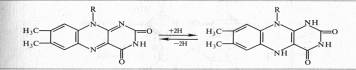
Примером дегидрогеназы, в состав которой входит ФАД, является сукцинатдегидрогеназа. Доноры электронов для аэробных дегидрогеназ — анаэробные дегидрогеназы, а акцепторы — хиноны, цитохромы, кислород.
Ранние люди
Древнейшими достоверно известными представителями человеческой линии эволюции были высокоразвитые двуногие человекообезьяны – австралопитеки и близкие к ним формы, которых обычно уже считают первыми людьми (гоминидами). Они появились в Восточной, а затем и в Южной Африке, в плиоцене – ок. 5–4 млн. лет назад. Возможно, что уже в одной из ...
Антигенсвязывающие центры антител
Согласно рентгеноструктурным исследованиям комплексов Fab-фрагментов с антигенами связывание антигена происходит в доступной растворителю щели активного центра, образованной вариабельными доменами в N-концевой части легкой и тяжелой цепей. Длина щели антител варьирует от 0,4 до 3,4 нм, а средние размеры области связывания для полимерных ...
Кислотность среды
Оптимальные значения рН для роста большинства дрожжеподобных грибов находится в области средней кислотности (рН4-6). Однако отдельные виды способны развиваться в более кислой среде. Например, некоторые штаммы Saccharomyces cerevisiae хорошо растут при рН 2,5-3.
Практически все виды дрожжей могут расти в диапазоне рН 4-4,5. В то же врем ...
